環境計量士試験では、気体の計算は 理想気体 を前提にする問題が中心ですが、ときどき ファンデルワールスの状態方程式 の意味を問う問題も出ます。
このとき意外と多いのが、
a と b の意味に毎回自信が持てない
という混乱です。
式は覚えていても、
- a が何を補正しているか
- b が何を補正しているか
が曖昧だと選択肢で迷いやすくなります。
ただ、この問題は計算量よりも、
どこが理想気体と違うのかを見抜けるか
が本質です。
計算問題全体の整理から確認したい方は、まずこちらの記事をご覧ください。
→ 環境計量士(濃度関係)計算問題の基本構造と5つの型
この記事で学べること
- ファンデルワールス式が理想気体式とどう違うか
- a と b が何を意味するか
- 本試験で選択肢をどう判断するか
問題(類題)
実在気体に対するファンデルワールスの状態方程式において、
定数 a と b が補正している内容として適切なものを説明せよ。
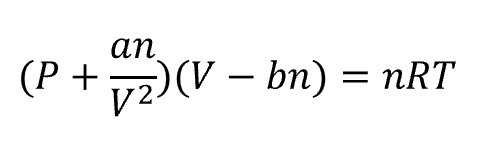
ただし、、P は気体の圧力、V は体積、T は絶対温度、𝑛は物質量、R は気体定数、
𝑎と𝑏 はファンデルワールス定数である。
解説
① 理想気体では何を無視しているか
理想気体では、
- 分子の大きさはない
- 分子同士の引力もない
と仮定します。
しかし実際の気体では、この2つは無視できません。
②基本となる考え方
理想気体では、状態方程式は下記のように表します。
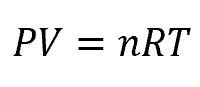
しかし実際の気体分子には、
- 分子同士の引力
- 分子自身の体積
いわゆる分子間相互作用があります。
そのため、理想気体の状態方程式では誤差が出ます。
a が補正するもの
a分子同士の引力があると圧力は小さく見える
分子が壁にぶつかう前に互いに引き合うため、
実際に壁へ与える圧力は理想気体より小さくなります。
その不足分を補うために、
圧力に足している
のが a 項です。
a は attraction(引力)
と覚えると整理しやすいです。
b が補正するもの
分子には大きさがある
ので、容器全体の体積すべてを自由に使えるわけではありません。
そのため、
実際に使える体積を小さくする
必要があります。
b は bulk(分子の大きさ)
と覚えると混同しにくくなります。
この問題の本質
この問題で問われるのは、
式変形ではなくどこを直しているか
です。
a は圧力側
b は体積側
これを位置で判断できると安定します。
試験で迷ったときの見方
式の中で、
足している方は圧力補正
引いている方は体積補正
です。
ここだけでも理解しておけばかなり楽になります。
よくある混乱
a と b を丸暗記だけで覚える
→ 緊張で試験中に自信が持てない、記憶があやふやになるのでおすすめできません。
圧力低下の理由が説明できない
→ 引力があるから壁への衝突が弱くなるのでその分を式としてプラスして補う、と理解しましょう。
体積補正の意味が曖昧
→ 分子そのものの体積を引く、とイメージしましょう。
まとめ
ファンデルワールスの状態方程式では、
- a は分子間引力による圧力補正
- b は分子の体積による体積補正
です。
試験では、
a = attraction
b = bulk
と結びつけて、
足しているか
引いているか
を見ると整理しやすくなります。
関連記事
環境計量士の計算問題に慣れるためには、次の基本パターンもあわせて確認しておくと整理しやすくなります。参考になれば幸いです。



コメント