環境計量士試験では、固体から気体への変化を扱う計算問題として ドライアイス の昇華が出題されることがあります。
この問題は、
- 密度
- 分子量
- mol
- 気体体積
が一度に出てくるため、最初にどこから手をつけるか迷いやすいテーマです。
ただし実際には、
密度が与えられている時点で入口が決まる
問題です。
密度は、
体積を質量に変えるためのヒント
だからです。
さらに、
1 cm³ と仮定することを思いつけばかなり整理しやすい
という特徴があります。
本記事では、令和6年 環境計量士(環化)試験の出題内容を参考に、一部数値を変更した類題を用いて、試験で止まらずに解くための考え方 を整理します。
計算問題全体の整理から確認したい方は、まずこちらの記事をご覧ください。
→ 環境計量士(濃度関係)計算問題の基本構造と5つの型
この記事で学べること
- 密度が与えられたときに最初に何を考えるか
- 1 cm³ を置いて倍率問題を簡単にする方法
- 固体から気体体積へ変換する基本手順
- 試験で迷わない判断の流れ
問題(類題)
二酸化炭素の固体(ドライアイス)が完全に昇華するとき、
0 ℃、1 atm において発生する気体の体積は、
ドライアイスの体積の何倍になるか求めよ。
ただし、
- 二酸化炭素の分子量:44
- ドライアイスの密度:1.6 g/cm³
- 0 ℃、1 atm における1 mol の体積:22.4 L
とする。
解説
① まず 1 cm³ と置く
「何倍か」を求める問題では、
1 cm³ を仮定すると最も簡単
です。
なぜなら最後に得られた気体体積を、そのまま倍率として読めるからです。
② 密度から質量を求める
密度 1.6 g/cm³ なので、1cm³ の質量は当然1.6 gです。
密度が与えられている=まず質量に変える
という流れを示しています。
③ 分子量を使って mol に変える
二酸化炭素の分子量は44なので、

④ 気体体積を求める
③でmol迄変換できたので、次に体積に変換します。
0℃、1atmにおける1molの体積は22.4Lなので、
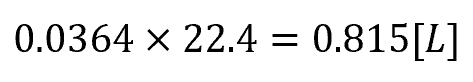
⑤ cm³ に戻す
1L=1000cm³ なので、
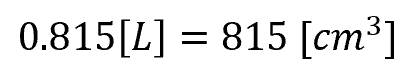
もともと1cm³ と仮定してここまで計算を進めてきているので、
815倍 が答えということになります。
この問題の本質
この問題で問われているのは、
計算そのものより、
密度を見た瞬間に入口を決められるか
です。
流れは毎回同じで、
密度→質量→mol→体積
この順番に乗せれば整理できます。
状態変化による倍数を求める問題では、
1 cm³ を置くと比が自然に見える
ため、途中で迷いにくくなります。
試験で止まりやすいポイント
密度をそのまま眺めて止まらない
密度は「gに変えられる」という合図です。
L と cm³ の変換を最後に忘れない
1 L = 1000 cm³ です。うっかり忘れないようにしましょう。
何倍問題はまず1単位で計算(今回だと1 cm³)
この発想でかなり整理できます。
まとめ
ドライアイスの昇華問題では、
- 1 cm³ を置く
- 密度で質量に変える
- mol を経由して気体体積へ進む
という一本道で考えられます。
試験では、
密度が出たらまず質量
と反応できると安定します。



コメント