電気分解の問題は、
式を覚えていても途中で何をすればよいか止まりやすい
分野です。
特に金属析出では、
どこまで単位を追えるか
で整理しやすさが大きく変わります。
今回のような問題では、
g → mol → 電子 mol → C → Q
と逆向きに考えると、
必要な式が自然に見えてきます試験の出題内容を参考に、一部数値を変更した類題を用いて、考え方と解き方を整理しています。
計算問題全体の整理から確認したい方は、まずこちらの記事をご覧ください。
→ 環境計量士(濃度関係)計算問題の基本構造と5つの型
この記事で学べること
- 電気分解を逆向きに整理する方法
- 電気量 Q の意味
- 電子 mol と金属 mol の関係
- ニッケル析出で 2 電子必要な理由
問題
硫酸ニッケル(Ⅱ)水溶液に銅板とニッケル板を浸漬させ、銅板を陰極、ニッケル板を陽極として、0.15 A の直流電流を8分間流した。
このとき、銅板にメッキされるニッケルの質量は何 g か。
ただし、
- ニッケルの原子量:58.7
- ファラデー定数:9.65×104 C/mol
とする。
解説
① まず逆向きに考える
求めたいのは g です。
したがって、
g を出すには mol が必要
です。
Ni の mol がわかれば、
原子量で g に直せます。
さらに Ni mol を出すには電子 mol
反応式は
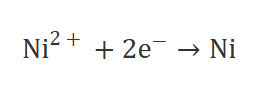
なので、
Ni 1 mol に電子 2 mol 必要
です。
電子 mol を出すには C
ファラデー定数は
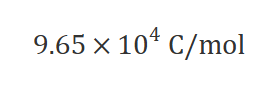
なので、
C がわかれば電子 mol にできる
です。
C を出すには Q=It
ここで電気量の式を使います。
つまり逆向きに見ると
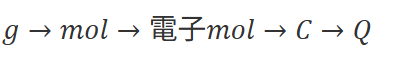
です。ここまでくればもう少しです。
② 電気量 Q を求める
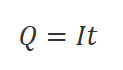
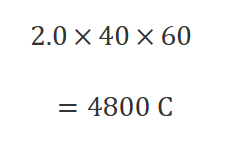
③ 電子 mol に直す
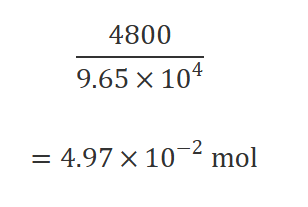
ここも単位を見ればわかりやすく、
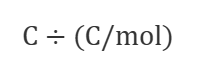
なので、
C が消えて mol が残る
ということです。
④ ニッケル mol に直す
Ni2+がNiになる反応では電子が2個反応に必要なので
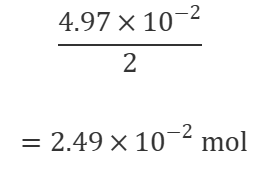
⑤ 質量に直す
最後に分子量をかけて質量に直せばおわりです。
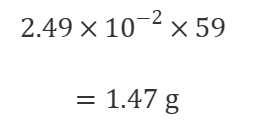
この問題の本質
この問題は、
順方向で覚えるより逆向きに単位で見る
と止まりにくくなります。
試験で落としやすいポイント
電子 mol のまま終わる
2電子を忘れる
時間を秒にしない
まとめ
電気分解では、
g → mol → 電子 mol → C → Q
と逆向きに見ると、
使う式が自然に決まる
ようになります。
試験では、
単位が次の一手を教えてくれる
と考えるとかなり安定します。
関連記事
他にも計算問題全般に関わる構造の解説や様々な計算問題の解説を行っています。
参考になれば幸いです。



コメント