環境計量士試験では、難しい計算問題やマイナーな知識問題を得点できるかよりも、
基本的な計算問題を確実に得点できるか が合否に大きく影響します。
今回のような 水酸化ナトリウム の問題は一見単純ですが、
- g/L を mol/L に直す
- 強塩基として扱う
- pOH と pH を取り違えない
という基本事項を落ち着いて処理する必要があります。
特に、
「完全電離としてよいか迷う」
受験者の方もいるので、本試験ではどのように判断するかもあわせて整理します。
(いやいやそれは迷わない・・楽勝でしょ、という方はぜひ別の記事をご覧ください(笑))
計算問題全体の整理から確認したい方は、まずこちらの記事をご覧ください。
→ 環境計量士(濃度関係)計算問題の基本構造と5つの型
この記事で学べること
この記事では次の3点を確認できます。
- g/L から mol/L へ変換する方法
- 強塩基の pH 計算の基本手順
- 本試験で迷わず完全電離と判断する考え方
問題(類題)
0.20 g/L の水酸化ナトリウム(NaOH)水溶液の pH を求めよ。
ただし、
- NaOH の分子量は 40
- 水のイオン積は [H⁺][OH⁻] = 1.0×10^-14
- log10 2.0 = 0.30
とする。
この問題のポイント
NaOH は強塩基なので、
NaOH → Na⁺ + OH⁻
として完全電離すると考えます。
ここで迷いやすいのは、
「完全電離としてよいのか?」
という点です。
本試験では、
もし電離度を考える必要がある場合や完全電離しない条件であれば、
- 電離度
- 平衡定数
- 弱塩基であること
などの前提が問題文に与えられます。
今回はそのような条件がなく、
与えられている情報だけで計算するなら、
完全電離を前提に単純な pH 計算をする問題
と判断してよいです。
(むしろ、この条件ではそう考えて解くしかありません。。。)
したがって、まず g/L を mol/L に変換し、そのまま OH⁻濃度とみなします。
①mol/Lへの換算
まず濃度を mol/L に直します。
NaOH の分子量は 40 なので、
0.20 g/L ÷ 40 g/mol = 0.0050 mol/L
したがって、
OH⁻濃度 = 0.0050 mol/L となります。
②pOHを求める
pOH = -log10(0.005) = -log10(5.0×10^-3)
log105.0 は、
log1010 – log102.0
として考えると、
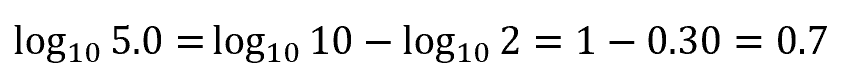
したがって、
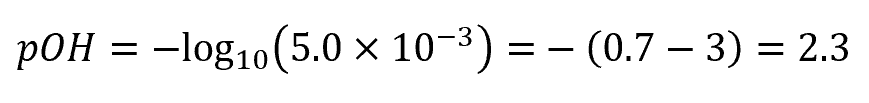
③pHへ変換
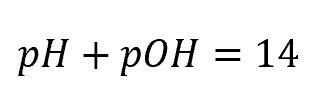
なので、
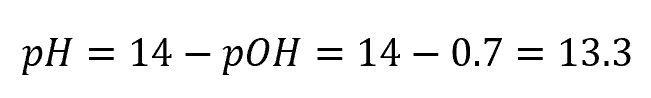
答え
pH = 11.7
この問題で落としやすいポイント
① g/L のまま計算してしまう
必ず mol/L に変換します。
② pOHで止まる
求めるのは pH です。
最後に14から引きます。
③ log の符号ミス
-log の処理でマイナス符号を落としやすいです。
この問題の本質
この問題で問われているのは、
g/L → mol/L → pOH → pH
の順番を崩さず進められるかです。
g/L を見たら、まず mol/L
と決めると止まりにくくなります。
試験で落としやすいポイント
① g/L のまま log に入らない
必ず mol/L に直します。分子量をきちんと確認しましょう。
② pOH で止まらない
実際の試験問題の選択肢も確認したらミスはしないと思いますが、求めるのは pH です。
気を付けましょう。
③ log の符号を落とさない
「-log」のマイナスを忘れないようにし、計算ミスをなくしましょう。
まとめ
この問題は、かなり基本的なサービス問題です。
難しい平衡計算ではなく、
- mol変換
- log処理
- pOH→pH変換
を落ち着いて処理すれば正解できます。
環境計量士では、
難問よりもまずこのレベルを確実に取ることが重要です。
関連記事
環境計量士の計算問題に慣れるためには、次の基本パターンもあわせて確認しておくと整理しやすくなります。参考になれば幸いです。



コメント