環境計量士試験では、沈殿滴定とあわせて 溶解度積(Ksp) を使う計算問題が出題されます。
この分野は、
- 当量点で何が残っているか分からなくなる
- Ag⁺ と Cl⁻ のどちらを使うか迷う
- 溶解度積の式は書けても次に進めない
という形で止まりやすいテーマです。
特に試験では、
「当量点=反応終了」でも、溶液中のイオンは完全にゼロではない
という理解が重要になります。
本記事では、令和4年 環境計量士(環化)試験の出題内容を参考に、一部数値を変更した類題を用いて、試験で止まらずに解くための考え方 を整理します。
計算問題全体の整理から確認したい方は、まずこちらの記事をご覧ください。
→ 環境計量士(濃度関係)計算問題の基本構造と5つの型
この記事で学べること
- 当量点で溶液中に何が存在するか
- 溶解度積からイオン濃度を求める方法
- この問題で本当に問われている本質
- 試験で迷わない判断手順
問題(類題)
塩化物イオンを含む試料水溶液に硝酸銀標準液を加えて沈殿滴定した。
この滴定の当量点において、水溶液(試料水溶液+標準液)中に溶解している塩化物イオンのモル濃度はいくらか。
ただし、塩化銀の溶解度積を
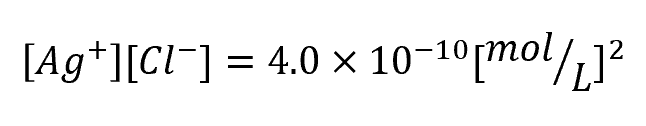
とする。
また、この沈殿生成以外の反応は起こらないものとする。
解説
① 当量点では何が起きているか
Ag+とCl–は
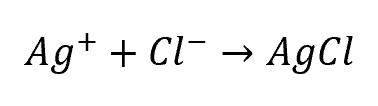
と反応して沈殿が発生します。
当量点とは、
加えた Ag⁺ の量
と
試料水溶液の Cl⁻ の量
がちょうど等しくなった点です。
つまり、
反応できる分はすべて沈殿した
状態です。
② それでも完全にゼロではない
ここがこの問題の最重要ポイントです。
沈殿した AgCl は、
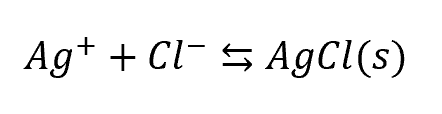
のように、
少しだけ溶ける
性質を持っています。
③イメージで考える
砂糖を水にたくさん入れると、底に砂糖が残ります。
でも、
水の中には少し砂糖が溶けている
状態ですよね。
AgCl も同じです。
沈殿していても少量は溶液中に存在する
だから当量点でも、
Ag⁺ と Cl⁻ は少し残る
のです。
④ なぜ Ag⁺ と Cl⁻ は同じ濃度か
AgCl が1分子が溶けると、
Ag⁺1個 と Cl⁻1個
が同時に出ます。
だから、
増える量は必ず同じ
です。
したがって、
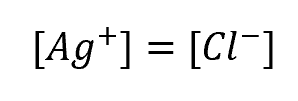
とおけます。
⑤ 溶解度積に代入する
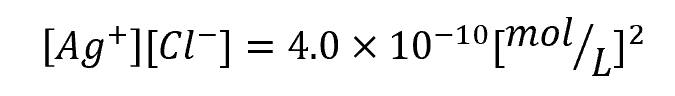
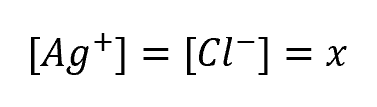
とすると、
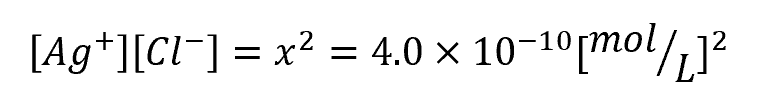
よって、
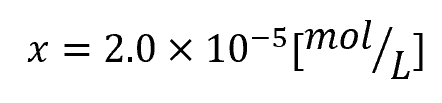
この問題の本質は何か
ここで試験が見ているのは、平方根計算そのものではありません。
本当に問われているのは、
当量点でも平衡が残る
と理解できるかです。
なぜ Ksp が与えられているのか
もし平衡状態が維持されず、完全にイオンの濃度がゼロなら
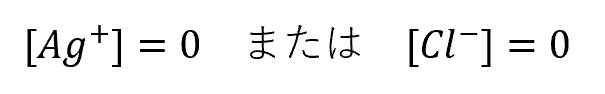
ということなので、
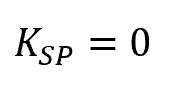
となり、問題文の設定と矛盾してしまいます。
ですが問題では Ksp が0以外の値で与えられています。
つまり、
少し溶けて平衡している前提
なのです。
試験で止まりやすいポイント
当量点=完全消失ではない
平衡状態なので、イオンの濃度はゼロにはなりません。
1:1 型沈殿なら x²
AgCl は典型的な1:1型の沈殿です。
Ksp が見えたら「少し残る」
このイメージが重要です。
この問題を見た瞬間の判断
次の語が並んだら溶解度積を使うと思い出しましょう。
Kspは問題文に与えられていると思うので見逃さないようにしましょう。
- 当量点
- 沈殿滴定
- AgCl
- 溶解度積
まとめ
溶解度積の問題では、
- 当量点でも少し溶ける
- 1:1なら濃度は等しい
- Ksp に代入して平方根
この流れで整理できます。
試験では、
「反応が終わった後に何が残るか」までイメージして問題に取り組む
ことが重要です。
関連記事
環境計量士の計算問題に慣れるためには、次の基本パターンもあわせて確認しておくと整理しやすくなります。参考になれば幸いです。



コメント