環境計量士(環化)の計算問題では、化学平衡の応用として錯体形成反応が扱われることがあります。
一見すると式が複雑ですが、
物質量の保存 → 平衡式 → 近似 の順で整理すると解けます。
今回は、安定度係数 Kを用いて、
平衡後に残る金属イオン濃度
を求める基本パターンを整理します。
本記事では、令和3年環境計量士(環化)試験の出題内容を参考に、
一部数値を変更した類題を用いて解説しています。
実際の試験問題とは数値が異なる場合がありますが、
考え方と計算手順はそのまま応用できます。
計算問題全体の整理から確認したい方は、まずこちらの記事をご覧ください。
→ 環境計量士(濃度関係)計算問題の基本構造と5つの型
この記事で学べること
- 錯体形成平衡の基本式
- 安定度係数 の使い方
- 平衡濃度の整理方法
- 高い安定度係数での近似計算
問題
金属イオン M の水溶液(濃度 0.03 mol/L)と、錯形成剤 L の水溶液(濃度 0.05 mol/L)を同体積ずつ混合した。
混合後、M と L は可溶な錯体 ML を形成し、平衡に達した。
錯体 ML の安定度係数を
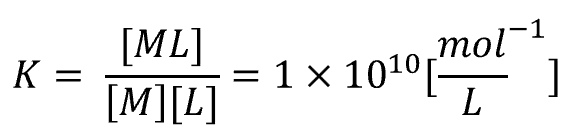
とする。
このとき、平衡状態で錯形成していない金属イオン M の濃度を求めよ。
ただし、この錯形成反応以外の反応は起こらないものとする。
解説
① まず混合後の初濃度を求める
同体積混合なので、濃度は半分になります(仮に1Lずつとイメージするとわかりやすいです)。
金属イオン M:

錯形成剤L:
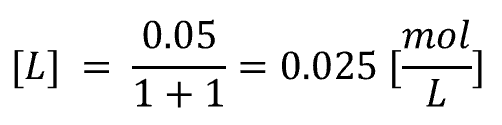
したがって初期状態は、
- M:0.015 mol/L
- L:0.025 mol/L
です。
② MとLのどちらが不足するか確認する
反応は
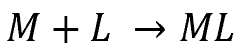
1:1で進みます。
M が 0.015 mol/L
L が 0.025 mol/L
なので、
M が先に使い切られる
と考えられます。
③ 錯体生成後の概算
M が全部錯体になると、
L は 0.015 消費されるので、
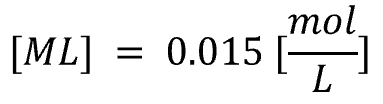
残る自由なLは濃度として、
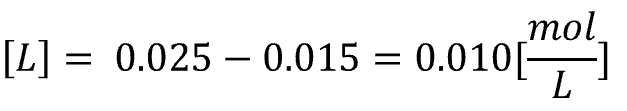
④ 安定度係数式へ代入する
安定度係数の式から、
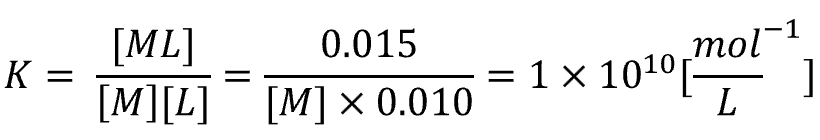
答え
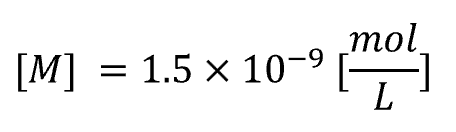
⑥ なぜこんなに小さくなるのか
安定度係数が 1010
と非常に大きいため、
M はほぼ完全に錯体になります。
つまり、
自由な金属イオンはほとんど残らない ということです。
⑦ 試験でのコツ
このタイプは、
何:何 で錯形成するのかを化学反応式から正しく判断し、
混合前、混合後の体積変化によって濃度が変わることに注意が必要です。
まとめ
- 同体積混合なら濃度は半分
- まず不足成分を確認する
- 化学反応式から反応mol比を正しく認識する
- 濃度は混合前と混合後で変わる(変わらない場合もあるかもしれないが変わると常に想定しておく)
関連記事
環境計量士の計算問題に慣れるためには、次の基本パターンもあわせて確認しておくと整理しやすくなります。参考になれば幸いです。



コメント