今回は、環境計量士試験で出題される
「理想気体の状態方程式を使う計算問題」
の具体例を解説します。
このテーマの基本構造は、別記事の
「環境計量士(濃度関係)|計算問題の基本構造と解き方」で整理しています。
理想気体の状態方程式 の問題では、
- 混合気体
- 体積%
- 圧力
が同時に出ると複雑に見えます。
ただし本質は、
総 mol が出れば終わり
です。
今回は、
体積% → 100 mol 仮定 → 質量 → 総 mol → 圧力
という順番で整理します。
本記事では、その考え方を使いながら
実際の試験レベルの問題を1問、ステップごとに解説していきます。
計算問題全体の整理から確認したい方は、まずこちらの記事をご覧ください。
→ 環境計量士(濃度関係)計算問題の基本構造と5つの型
この記事で学べること
- 体積%をモル比として使う理由
- 平均分子量を式暗記なしで出す方法
- 混合気体問題の基本の流れ
※補足
本記事では、令和6年 環境計量士(環化)試験の出題内容を参考に、
一部数値を変更した類題を用いて解説しています。
問題
窒素の体積百分率80%、酸素の体積百分率20%の混合気体28.8 gを、
10 Lの密閉容器に入れ、35℃に保った。
このとき、容器内の圧力を求めよ。
条件
- 窒素の分子量:28
- 酸素の分子量:32
- 気体定数
R = 8.3 × 10³ (Pa・L・K⁻¹・mol⁻¹)
解き方のポイント
この問題で最初に見るのは、
体積% = モル比
です。
理想気体では、
同温同圧なら
体積 ∝ mol
だからです。
つまり、
N₂ : O₂ = 80 : 20
とそのまま mol 比で使えます。
① 理想気体の状態方程式
理想気体は次の式で表されます。
PV = nRT
今回求めたいのは 圧力 P なので、式を変形すると
P = nRT / V
となります。
つまり、この問題では
総モル数 n が分かれば圧力を求めることができる
ということになります。
② 体積百分率=モル比になる理由
理想気体の状態方程式
PV = nRT
を見ると、温度 T と圧力 P が同じ条件では
V ∝ n
つまり
体積はモル数に比例する
ことが分かります。
したがって、混合気体では
Vi / Vtotal = ni / ntotal
という関係が成り立ちます。
つまり
体積百分率 = モル百分率
として扱うことができます。
今回の混合気体では
- 窒素:80 %
- 酸素:20 %
なので
nN₂ : nO₂ = 0.8 : 0.2
というモル比になります。
③ 混合気体の平均分子量を求める
体積百分率がモル比になるので、
混合気体の平均分子量は次の式で求められます。
Mmix = yN₂MN₂ + yO₂MO₂
ここで
- y:モル分率
- M:分子量
です。
数値を代入すると
Mmix = 0.8 × 28 + 0.2 × 32
= 22.4 + 6.4
= 28.8
したがって、この混合気体の平均分子量は
28.8 g/mol
となります。
④ 総モル数を求める
総質量は
28.8 g
なので
n = m / M
より
n = 28.8 / 28.8
n = 1.0 mol
となります。
⑤ 圧力を求める
理想気体の式
P = nRT / V
に値を代入します。
n = 1
R = 8.3 × 10³
T = 35℃ = 308 K
V = 10 L
P = (1 × 8.3 × 10³ × 308) / 10
P = 2.556 × 10⁵ Pa
したがって
容器内の圧力は
約 2.56 × 10⁵ Pa
となります。
この問題の本質
この問題の本質は 混合気体の平均分子量 にあります。
混合気体では
Mmix = Σ (yi Mi)
という式が成り立ちます。
平均分子量が求まれば
n = m / Mmix
で総モル数を求めることができ、
そのまま理想気体の状態方程式
P = nRT / V
に代入することで圧力を求めることができます。
このように、混合気体の問題では
体積割合 → モル比 → 平均分子量 → 総モル数
という流れで考えると、スムーズに解くことができます。
別解(今回については楽な方法)
今回の問題については、平均分子量の式を覚えていなくても解くことが可能です。
その解き方を別解として記載します。
① 100 mol と仮定する
実は、
合計のmol数を100 mol と置く
と計算が一気に見えます。
窒素と酸素のmol数は下記になります。
- N₂ = 80 mol
- O₂ = 20 mol
② 100 mol の質量を出す
N₂は
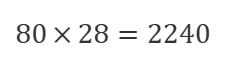
O2は
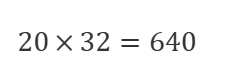
よって合計は2880gとなります。
つまり100 mol で 2880 g
なので、
平均分子量 = 28.8 g/mol
が自然に見えます。
③ 総 mol を求める
実際の質量は 28.8 g なので、n=28.828.8 =1.0 mol
④ 圧力を求める
これで圧力は求まります。
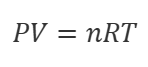
を変換して
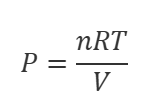
各数値を代入すると、
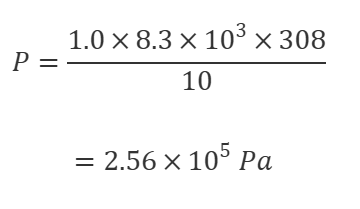
あわせて読みたい記事
環境計量士の計算問題を他にも解説していますので参考になれば幸いです。
また環境計量士の計算問題に共通して言える基本構造を整理した記事もあります。



コメント