環境計量士(環化)の計算問題では、
- 滴定
- イオン交換樹脂
- 洗液
- 標準液
が同時に出てくると、一気に難しく見えることがあります。
滴定はできる人は情報整理してパッとできてしまいますが、苦手な人は結構苦手です。
私も最初は苦手なタイプの問題でした。。。
ただ本質は、
最後に滴定した NaOH が何 mol の H⁺ に対応するか
だけです。
つまり、
最後に測れた mol を逆向きに戻す
と整理すると解きやすくなります。
今回は、令和7年 環境計量士(環化)試験の出題内容を参考に、一部数値を変更した類題で解説します。
計算問題全体の整理から確認したい方は、まずこちらの記事をご覧ください。
→ 環境計量士(濃度関係)計算問題の基本構造と5つの型
この記事で学べること
- 陽イオン交換樹脂で Cu²⁺ が H⁺ にどう対応するか
- 滴定結果から元の濃度を逆算する考え方
- 長文の計算問題でも、どこを見れば整理できるか
交換樹脂が出ても、最後に滴定しているものから逆にたどると整理しやすくなります。
問題(類題)
濃度不明の硫酸銅(Ⅱ)水溶液 20 mL を H⁺形陽イオン交換樹脂カラムに通し、さらに水でカラムを洗浄した。
これらの洗液を含む通過液をすべて集めて 0.10 mol/L の水酸化ナトリウム標準液で滴定したところ、中和に 10.0 mL を要した。
元の硫酸銅(Ⅱ)水溶液のモル濃度を求めなさい。
ただし、硫酸銅(Ⅱ)水溶液中の Cu²⁺ はすべて H⁺ に交換されたものとする。
この問題のポイント
最後に何を滴定しているか
です。
NaOH が中和するのは、
H⁺
です。
したがって、
イオン交換樹脂から出た H⁺ の総量
を求めればよいことになります。
そもそも陽イオン交換樹脂で起こることは?
陽イオン交換樹脂は文字通り、
陽イオンを交換 する樹脂です。
そして交換するための素材がH+であるため、
H+形陽イオン交換樹脂 と呼ばれます。
硫酸銅(Ⅱ)は水中で次のように電離します。
(「(Ⅱ)」と書いている部分がヒントになりますね。この(Ⅱ)の部分がCuの価数です)
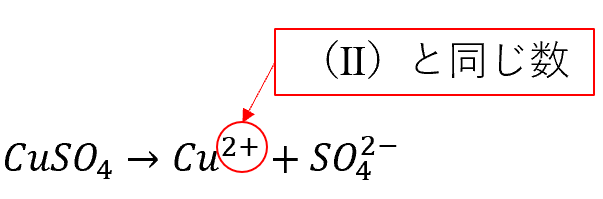
H⁺形陽イオン交換樹脂ではCu²⁺ が樹脂に保持され、
代わりに H⁺ が放出されます。
Cu²⁺ は 2価なので、
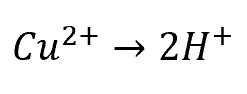
※ここでは化学反応式ではなく、Cu²⁺ 1 mol に対して H⁺ が 2 mol 放出される対応関係を簡略的に示しています。
「硫酸銅(Ⅱ)水溶液中の Cu²⁺ はすべて H⁺ に交換されたものとする」という記載があるので、
Cu²⁺ は 2H⁺ と等価交換される ということです。
NaOHの物質量を求める
濃度 0.10 mol/L
使用量 10.0 mL = 0.01 L なので、NaOHの物質量は
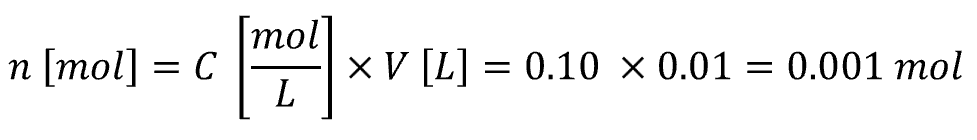
NaOHの物質量と交換されるH+の物質量は同じになるので、
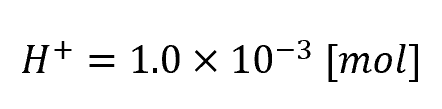
Cu²⁺ の物質量へ戻す
Cu²⁺ 1 mol に対して H⁺ 2 mol で等価交換になるので、
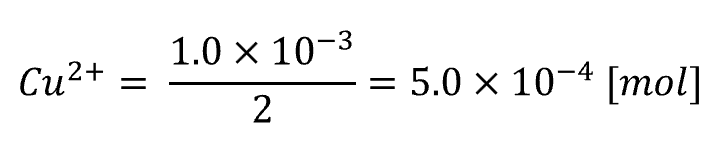
元の濃度を求める
試料は 20 mL = 0.020 Lなので、
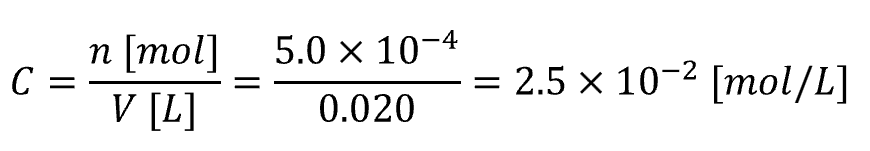
答え
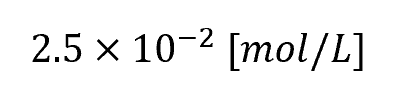
よくあるミス
Cu²⁺ と NaOH を1:1にしてしまう
Cu²⁺ は 2価なので、H⁺ 2個分に対応します。
ここが最重要ポイントです。
焦ると1:1で計算してしまう可能性があるので気を付けましょう。
洗液が加わって体積は増えていると考え濃度計算を間違える
必要なのは濃度ではなく、H⁺ の総 mol 数です。
滴定で直接数えているのは、全体に何 mol 含まれているか
なので、
薄まっても総量は変わらない
このタイプの問題の見抜き方
長文でも最初に確認するのは2つだけです。
- 最後に何を滴定しているか
- イオンが何価か
この問題では、
- NaOH → H⁺を見る
- Cu²⁺ → H⁺ 2個
これで解けます。
まとめ
この問題は、
最後に測れた mol を逆向きに戻す
だけです。
- NaOHで滴定しているのは H⁺
- Cu²⁺ 1 mol に対して H⁺ は 2 mol 放出される
- 最後に試料体積で割って濃度を求める
という流れを押さえれば整理できます。
陽イオン交換樹脂が登場すると複雑に見えますが、
最終的に何を滴定しているかを確認すると、必要な計算はシンプルです。
落ち着いて解くことで得点源にしていきましょう!
あわせて読みたい記事
陽イオン交換樹脂の問題では、
- 物質量の計算
- イオンの価数
- 滴定結果の読み取り
が組み合わさります。
環境計量士の計算問題に慣れるためには、次の基本パターンもあわせて確認しておくと整理しやすくなります。参考になれば幸いです。



コメント