環境計量士(環化)の計算問題では、熱化学分野からヘスの法則を利用する問題が出題されることがあります。
その中でも代表的なのが格子エンタルピーです。
格子エンタルピーは直接測定しにくいため、
- 昇華
- 結合の解離
- 電子放出
- 電子付加
といった複数の反応を組み合わせて求めます。
一見すると数値が多く複雑に見えますが、
どの反応を足して、どこを引くかを整理できれば確実に得点できます。
今回は、CaF₂を例に、熱化学サイクルから格子エンタルピーを求める手順を整理します。
本記事では、令和7年環境計量士(環化)試験の出題内容を参考に、
一部数値を変更した類題を用いて解説しています。
実際の試験問題とは数値が異なる場合がありますが、
解法の流れはそのまま応用できます。
計算問題全体の整理から確認したい方は、まずこちらの記事をご覧ください。
→ 環境計量士(濃度関係)計算問題の基本構造と5つの型
この記事で学べること
- 格子エンタルピーの意味
- ヘスの法則による熱化学サイクルの考え方
- 各エンタルピー値をどう整理するか
- 試験で符号ミスを防ぐ方法
問題
ふっ化カルシウム CaF₂(s) から気体のカルシウムイオン Ca²⁺(g) と気体のふっ化物イオン F⁻(g) が生成する反応のエンタルピー変化(格子エンタルピー)ΔH_lattice を求めよ。
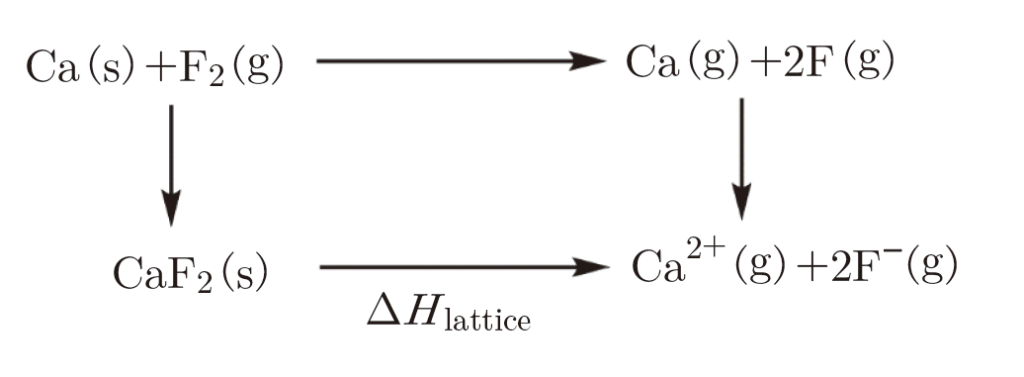
各過程のエンタルピー変化 ΔH は次のとおりとする。
| 過程 | 反応式 | ΔH / kJ mol⁻¹ |
|---|---|---|
| CaF₂(s)の生成 | Ca(s) + F₂(g) → CaF₂(s) | −1200 |
| Ca(s)の昇華 | Ca(s) → Ca(g) | 178 |
| F₂(g)の解離 | F₂(g) → 2F(g) | 159 |
| Ca(g)の電子放出 | Ca(g) → Ca⁺(g)+e⁻ | 590 |
| Ca⁺(g)の電子放出 | Ca⁺(g) → Ca²⁺(g)+e⁻ | 1145 |
| F(g)の電子付加 | F(g)+e⁻ → F⁻(g) | −328 |
① そもそも何を作りたいのかを整理する
最終的に求めたいのは、
です。
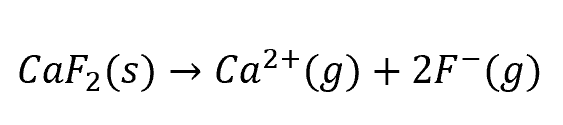
つまり、
固体イオン結晶を完全に気体イオンへ分解するエネルギー
です。
固体結晶を完全に気体イオンへばらす
エネルギーです。
直接その反応は与えられない
ので、
足りない反応を順にたどって埋める
と考えます。
便宜上、それぞれのエンタルピーを図のように設定します。
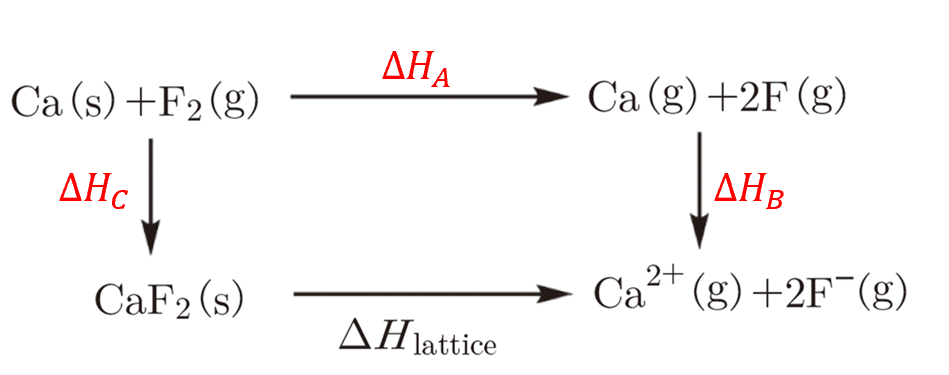
② 元素を気体原子にする(ΔHA)
まずCa(s)を気体にします。
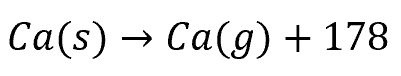
次にF₂を原子へ分解します。
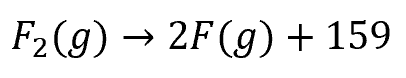
③ カルシウムを2価陽イオンにする(ΔHB)
1回目の電子放出:
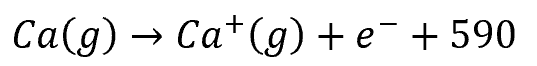
2回目の電子放出:
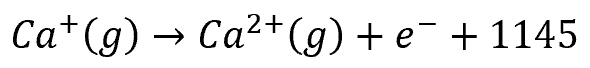
④ フッ素原子へ電子を与える(ΔHB)
1個のF原子に電子を与えると:
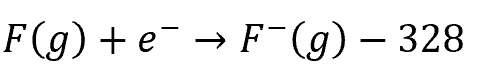
F2であり、F原子は2個あるので:
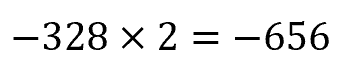
⑤ ここまで全部足す(ΔHA+ΔHB)
ここまでで計算した個別のエネルギー計算についてすべて足して計算します。

⑥ 生成エンタルピーと関係をつなぐ(ΔHC)
CaF₂生成は:
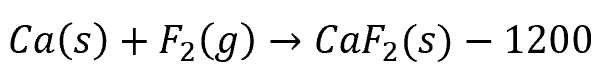
です。
ヘスの法則より、
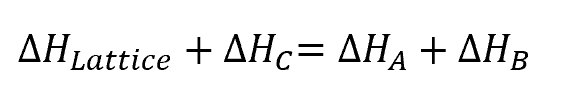
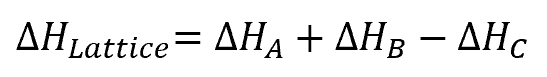
答え
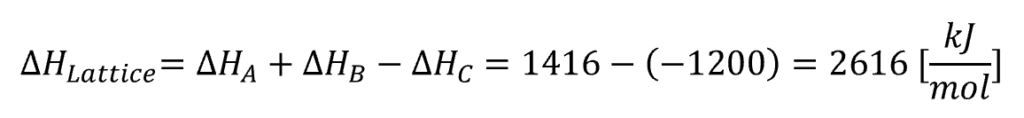
⑦ なぜ最後に「引く」のか
ここで迷いやすいのが符号です。
生成エンタルピーは、元素から結晶を作るときに放出される熱です。
今回求めるのは逆方向なので、
逆向き=符号反転
となります。
ここが焦るとよく発生するミスです。
まとめ
- 格子エンタルピーは直接求めずヘスの法則で計算する
- 前提となる各過程のエンタルピーの式は与えられていることが多いので、落ち着いて各反応を順番に足して整理する
- 生成エンタルピーは最後に逆向きで使うことがあるので注意。反応式の矢印の向きをよく確認する。
- 試験では符号ミス防止が最重要



コメント