環境計量士(環化)の計算問題では、
- 化学式が長い
- 設定が見慣れない、過去問で見たことがない
- 文章が長い
というだけで難しく感じる問題があります。
令和7年に出題されたメタンハイドレートもその一つですが、
実際には
1 mol の 水和物 から水とメタンが何 mol 出るか
を整理するだけです。
今回は、令和7年 環境計量士(環化)試験の出題内容を参考に、一部数値を変更した類題で解説します。
計算問題全体の整理から確認したい方は、まずこちらの記事をご覧ください。
→ 環境計量士(濃度関係)計算問題の基本構造と5つの型
この記事で学べること
- 式量から水分子数を求める考え方
- 水の生成量から元の物質量へ戻す方法
- ケージ占有率 α の使い方
文章が長くても、1 mol あたりの関係に戻すと整理しやすくなります。
問題(類題)
メタンハイドレートは水分子が作るかご状構造の中にメタン分子が包接された構造をもつ。
メタンハイドレートの化学式はαCH4・𝑛H2O で表され、1 mol のメタンハイドレートが分解するとα mol のメタンと𝑛 mol の水を生じる。α はケージ占有率(水分子が作るかごにメタン分子が入っている割合)であり、理想構造においてはα = 1.0 である。
ある天然メタンハイドレート(α = 0.90)を分解したところ、0.90 kg の水が生成した。
このとき発生するメタンは何 mol か求めなさい。
ただし、天然メタンハイドレート(α = 0.90)の式量は122.4、
メタンおよび水の分子量はそれぞれ16 と18、水の比重は1.0 とする。
メタンハイドレートの基本式
メタンハイドレートは問題文の通り、次のように表されます。
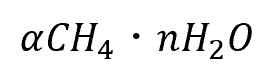
今回は α = 0.90 です。
まず n を求める
ここで重要なのは、
水が何 mol 含まれる 水和物 かを先に決める
ことです。
これがわからないと、
後で水 mol から戻せない
からです。
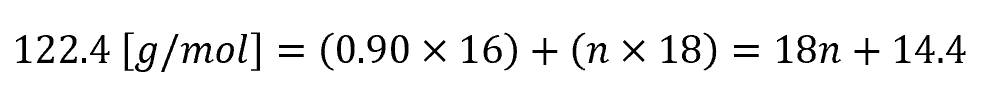
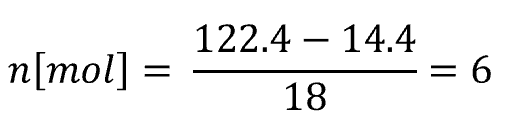
つまり、メタンハイドレートは0.9CH4・6H2O と表すことができる、ということになります。
水0.90kgを mol に変換する
これは単純に、
0.90 kg = 900 g なので、
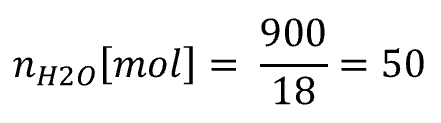
メタンハイドレートの mol を求める
問題文の「1 mol のメタンハイドレートが分解するとα mol のメタンと𝑛 mol の水を生じる。」とnが6であることから、
1 mol のメタンハイドレート → 6 molの水分子 ですので、メタンハイドレートのmol数は、
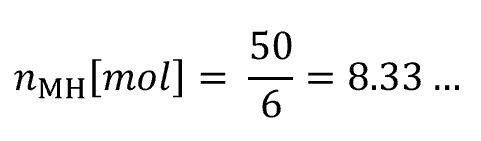
メタンのmol数を求める
αが0.9であることから、1 mol のメタンハイドレート → メタン0.90 mol という意味なので、
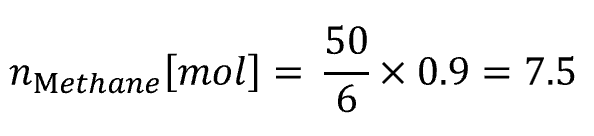
答え
発生するメタンのmol数は 7.5mol となります。
よくあるミス
よく読まずにα=1.0を使って計算してしまう
問題を解くのに使うのはα=0.9です。気を付けましょう。
メタンmol数計算で0.9をかけずに割ってしまう
ケアレスミスはもったいないので計算結果に不自然さを感じたら丁寧に見直しましょう。
このタイプの問題の見抜き方
長文問題では、
- 未知数と既知数を明確に整理する
- 計算に使う数値を確実に問題文から拾う
などが有効です。
まとめ
今回の問題では、
- 式量から n を求める
- 水 のmol数 から メタンハイドレートの mol数 を求める
- α を掛けてメタン mol を出す
という順番で整理できます。
文章が長くても、mol の対応関係を考えて整理すると計算しやすくなります。
あわせて読みたい記事
環境計量士の計算問題を他にも解説していますので参考になれば幸いです。
また環境計量士の計算問題に共通して言える基本構造を整理した記事もあります。



コメント