環境計量士試験では、溶液の性質に関する計算問題として ラウールの法則 が出題されることがあります。
この分野は、
- モル数に直すところで止まる
- 分母に何を入れるか迷う
- 蒸気圧低下の意味が曖昧になる
という形で苦手意識を持ちやすいテーマです。
特に試験では、
「溶質は蒸発しない」
という前提を使って整理できるかが重要になります。
本記事では、令和6年 環境計量士(環化)試験の出題内容を参考に、一部数値を変更した類題を用いて、試験で止まらずに解くための考え方 を整理します。
計算問題全体の整理から確認したい方は、まずこちらの記事をご覧ください。
→ 環境計量士(濃度関係)計算問題の基本構造と5つの型
この記事で学べること
- ラウールの法則で蒸気圧を求める手順
- モル分率の作り方
- この問題で本当に問われている本質
- 試験で迷わない考え方
問題(類題)
11.4 g のスクロース(分子量342)を 90 g の水に溶かした。
この水溶液の 25 ℃ における水蒸気圧を求めよ。
ただし、
- 純水の蒸気圧:3.17 kPa
- スクロース水溶液はラウールの法則に従う
ものとする。
解説
① まず水とスクロースをモル数に直す
スクロース
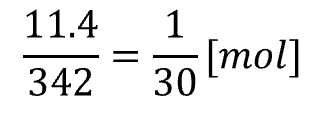
水
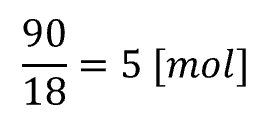
② 水のモル分率を求める
ここでは、
水蒸気圧を求めるので、溶媒(水)のモル分率 が必要です。
水のモル分率は、
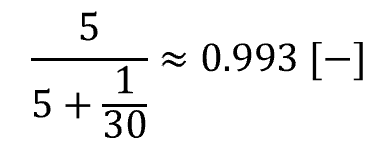
③ 蒸気圧を求める
ここでラウールの法則を適用します。
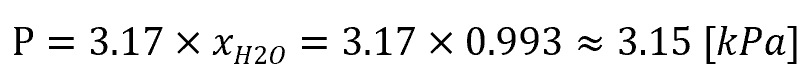
この問題の本質は何か
ここで試験が見ているのは、
11.4 g や 90 g の計算そのものではありません。
本当に問われているのは、
ラウールの法則の法則は不揮発性溶質の液体に適用するため「蒸発するのは水だけ」
と整理できるかです。
なぜスクロースは蒸気圧に直接入らないのか
スクロースは不揮発性です。
つまり、気相へ出るのは水だけです。
そのため、
水の割合(モル分率)が減る→蒸気圧が下がる
という構造になります。
なぜ分母にスクロースも入るのか
ここは注意が必要です。
蒸気圧は水だけですが、
モル分率は水溶液全体における比率なので、
全粒子数(全物質のmol)で割る
ので、
スクロースも分母に入ります。
試験で止まりやすいポイント
水またはスクロースのmol換算で割り切れず焦る
基本的に試験本番では割り切れることが多いですが、保証されているわけではありません。
g→mol換算時に割り切れなくても焦らずに計算を進めていきましょう。
モル分率
この問題を見た瞬間の判断
次の語が並んだらラウールの法則を思い出しましょう。
- 蒸気圧
- 純水の蒸気圧
- 分子量
- 水溶液
実際の試験では、今回の問題のように、
〇〇はラウールの法則に従う
と記載があることがほとんどなので、見逃さないように注意しましょう。
まとめ
ラウールの法則では、
- まず mol に直す
- 水のモル分率を作る
- 純溶媒(今回は水)蒸気圧を掛ける
この3段階です。
試験では、
「蒸発するのは誰か」を先に見る
と整理しやすくなります。
関連記事
環境計量士の計算問題に慣れるためには、次の基本パターンもあわせて確認しておくと整理しやすくなります。参考になれば幸いです。



コメント